Atomic structure: isotopes and radioactivity [EN❀ES]

Discovery of neon isotopes: in the lower right corner of this photographic plate by Joseph John Thomson, the two isotopes of neon are marked: neon-20 and neon-22
Descubrimiento de los isótopos de neón: en la esquina inferior derecha de esta placa fotográfica de Joseph John Thomson están marcados los dos isótopos del neón: neón-20 y neón-22
“…is used to indicate that all types of atoms of the same chemical element (isotopes) are found at the same place in the periodic table. Atoms that are isotopes of each other are those that have the same atomic number (number of protons in the nucleus), but different mass numbers (sum of the number of neutrons and the number of protons in the nucleus). The different isotopes of an element differ, therefore, in the number of neutrons…” ❀ Isotopes

“…se usa para indicar que todos los tipos de átomos de un mismo elemento químico (isótopos) se encuentran en el mismo sitio de la tabla periódica. Los átomos que son isótopos entre sí son los que tienen igual número atómico (número de protones en el núcleo), pero diferente número másico (suma del número de neutrones y el de protones en el núcleo). Los distintos isótopos de un elemento difieren, pues, en el número de neutrones…” ❀ Isótopos

Así como lo expone el anterior concepto, son los diversos átomos de un mismo elemento que se diferencian en su peso atómico. Esto se debe al hecho de estar constituidos sus núcleos por igual número de protones (igual número atómico Z), pero distinto número de neutrones. El número de electrones debe ser, naturalmente, igual al número de protones, para que se mantenga la neutralidad del átomo.
Recent studies on the atomic structure of the elements have shown that, of the 104 elements known to date, only 21 are pure; thus, most of the elements in the periodic table are made up of a mixture of isotopes. According to several experiments, the isotope is radioactive when the ratio between the number of neutrons and protons is not appropriate to obtain nuclear safety or stability.
Recientes estudios sobre la estructura atómica de los elementos han puesto de manifiesto que, de los 104 conocidos hasta el momento, tan sólo 21 de ellos son puros; así, la mayor parte de los elementos que integran la tabla periódica están formados por una mezcla de isótopos. De acuerdo a varios experimentos realizados, el isótopo es radiactivo cuando no es apropiada la relación entre el número de neutrones y protones con la cual se obtiene la seguridad o estabilidad nuclear.

En 1912-1913, Frederick Soddy y Kasimir Fajans (cada uno por su parte), enunciaron los dos siguientes leyes, que llevan sus nombres: 1) Sí un elemento se desintegra emitiendo rayos alfa, su masa atómica disminuye en 4 unidades y su número atómico disminuye en 2 unidades. 2) Sí un elemento se desintegra emitiendo rayos beta, su masa atómica no varía pero su número atómico aumenta en una unidad.
This can be easily explained by taking into account that alpha particles have mass equal to 4 and a double positive charge, and that beta particles (electrons) have negligible mass and a negative charge.
Esto se puede explicar fácilmente teniendo en cuenta que las partículas alfa tienen masa igual a 4 y una doble carga positiva, y que las partículas beta (electrónes) tienen masa despreciable y una carga negativa.
Therefore, if an element successively undergoes one alpha disintegration and two beta disintegrations, it must again give an element with the same atomic number, thus occupying the same place in the periodic table, although now its mass is different from the original element; this is why these atoms are called isotopes.
Por lo tanto, si un elemento sufre sucesivamente una desintegración alfa y dos desintegraciones beta, debe dar nuevamente un elemento con el mismo número atómico, ocupando por consiguiente el mismo lugar en la tabla periódica, aunque ahora su masa es distinta del elemento originario; por eso se le llaman isótopos a estos átomos.

Some isotopes of the elements nickel (Ni), copper (Cu) and zinc (Zn). As in most isotope tables, the elements are arranged from bottom to top according to their increasing atomic number, and the isotopes from left to right according to their increasing mass. Color black: stable isotopes; blue: negative beta-emitting isotopes; red: positive beta-emitting isotopes.
Algunos isótopos de los elementos níquel (Ni), cobre (Cu) y zinc (Zn). Como en la mayoría de las tablas de isótopos, los elementos se organizan de abajo hacia arriba según su número atómico creciente, y los isótopos de izquierda a derecha según su masa creciente. Color negro: isótopos estables; azul: isótopos emisores de partículas beta negativo; rojo: isótopos emisores de partículas beta positivo.
El conjunto de los isótopos de un elemento se denomina Pléyade. Para el hidrógeno, por ejemplo, la pléyade consta de tres isótopos: el Protio o hidrógeno propiamente dicho, cuyo núcleo está formado por un solo protón; el Deuterio que presenta un núcleo integrado por un protón y un neutrón, y el Tritio, de cuyo núcleo entran a formar parte un protón y dos neutrones.

Thus, there are two types of isotopes:
Natural Isotopes: these are those found in nature, such as hydrogen, which has three natural isotopes: protium, deuterium and tritium. The latter is widely used by military scientists to manufacture the hydrogen nuclear bomb. Carbon is another very important element which is formed by natural isotopes.Artificial Isotopes: these are produced in nuclear laboratories bombarded with subatomic particles; they have a short life due to their radioactivity and instability. In nuclear technology, uranium-233 isotopes are used; another of these artificial isotopes is Iridium-192, used in the welding of pipes that transport oil (crude oil) or fuel, which is used to check the airtightness of the conductive pipe.
Así se presentan dos tipos de isótopos:
Isótopos Naturales: son los que se localizan en la naturaleza, como el hidrógeno, el cual posee tres isótopos naturales: protio, deuterio y tritio. Este último es muy usado por los científico militares para fabricar la bomba nuclear de hidrógeno. El carbono es otro elemento muy importante el cual está formado por isótopos naturales.
Isótopos Artificiales: son los que se producen en los laboratorios nucleares bombardeados con partículas subatómicas; los cuales poseen vida corta debido a su radioactividad y la inestabilidad que manifiesta. En la tecnología nuclear se usan los isótopos de uranio-233; otro de estos isótopos artificiales es el Iridio-192, usado en las soldaduras de tubería que transportan petróleo (crudo) o combustible, con el se comprueba lo hermético del tubo conductor.
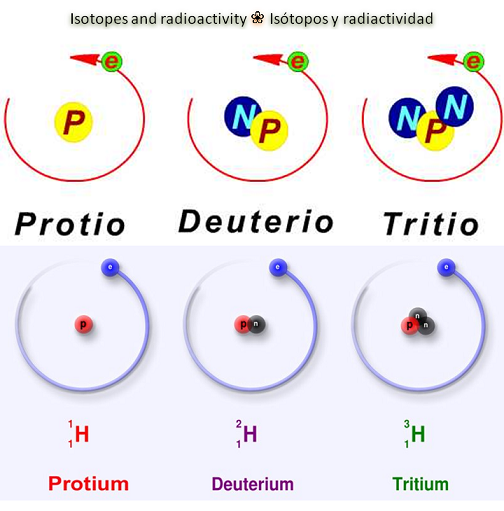
Hydrogen isotopes diagram / Diagrama de los isótopos del hidrógeno
Existen ciertos isótopos de algunos elementos a partir de cuyos núcleos puede conseguirse la emisión de partículas y radiaciones dando lugar a una variación en la constitución del mismo. Este fenómeno, denominado Radiactividad, fue descubierto por Henri Becquerel, quién a finales del siglo XIX, observó que las Sales de Uranio emitían una radiación penetrante que llagaba a impresionar una placa fotográfica después de atravesar una superficie absorbente de radiaciones que las envolvía. Los trabajos de los esposos Joliot-Curie dieron como fruto la obtención de otros elementos que se comportan de forma análoga al uranio: el Polonio y el Radio. A lo largo del siglo XX se ha conseguido detectar otros isótopos de elementos radiactivos, caracterizados por un comportamiento químico similar.
The radiation emitted by these substances is characterized, as has been said, by impressing photographic plates when passing through non-transparent solid bodies, thus offering the possibility of obtaining radiographs similar to those obtained by means of X-rays; they also produce intense ionization when passing through gaseous masses and induce phosphorescent and fluorescent luminosity. These, together with many other properties, make natural radioactivity one of the facets of chemistry with the largest and widest fields of application.
La radiación emitida por estas sustancias se caracteriza, como se ha dicho, por impresionar placas fotográficas al atravesar cuerpos sólidos no transparentes, por lo que ofrece la posibilidad de conseguir radiografías similares a las obtenidas por medio de Rayos X; producen, asimismo, una intensa ionización al atravesar masas gaseosas e inducen luminosidad fosforescente y fluorescente. Estas, junto con otras muchas propiedades, hacen de la radiactividad natural una de las facetas de la química con más y mayores campos de aplicación.

La radiación que emiten las sustancias radiactivas consta de tres tipos de rayos de diferente naturaleza: - Rayos o Partícula α transportan partículas de carga positiva similares a los núcleos de Helio, es decir, de: Z = 2 y A = 4 - Rayos o Partícula β están constituidos por partículas elementales de carga negativa y su masa es mucho menor que las radiaciones de tipo α - Rayos Gamma o Rayos ץ son radiaciones electromagnéticas de longitud de onda muy corta y, por consiguiente, de gran poder de penetración.

Information from the article: Isotopes
El estudio de los isótopos ha sido observado principalmente para los elementos radioactivos, en los que los isótopos están más o menos bien separados; pero luego, la noción se ha extendido al resto de los elementos químicos.
The simple substances of chemistry are, in reality, mixtures of elementary constituents designated by the name of isotopes. Experiments in transmutation and artificial radioactivity have made it possible to obtain new isotopes from neighboring elements.
Las sustancias simples de la química son, en realidad, mezclas de los constituyentes elementales que se designan con el nombre de isótopos. Las experiencias de transmutación y de radioactividad artificial han permitido obtener nuevos isótopos a partir de elementos vecinos.
This phenomenon has also led to the need to define two scales of atomic weights: the chemical scale, in which the atomic weight of the natural mixture of oxygen isotopes is adopted as 16.0000; and the physical scale, in which the atomic weight of the oxygen isotope of mass number 16 (i.e., 8 protons and 8 neutrons) is adopted as 15.878. The conversion factor from chemistry to physics is: 1.000279.
Este fenómeno ha dado lugar también a que haya que definir dos escalas de pesos atómicos: la escala química, en la que se aopta como peso atómico de la mezcla natural de isótopos de oxígeno el valor 16,0000; y la escala física, en la que el peso atómico del isótopo del oxígeno de número de masa 16 (es decir, de 8 protones y 8 neutrones) se adopta como 15,878. El factor de pasaje de la química a la física, es: 1,000279.
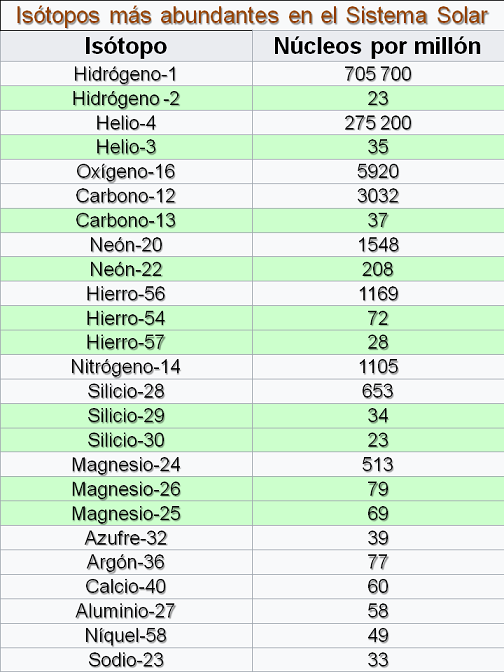
(Data originating from article: Isotopes)

¡ SIEMPRE GRACIAS
POR SU AMABLE ATENCIÓN !
POR SU AMABLE ATENCIÓN !
ALWAYS THANK YOU
FOR YOUR LOVING CARE !
FOR YOUR LOVING CARE !

I dedicate this report to the educational and cultural training of everyone who knows its importance and respects the value of integral education
Dedico este informe a la formación educativa y cultural de todo aquel que conoce su importancia y respeta lo valioso de la educación integral
❀ @maria1989 ❀
Artículos de consulta / Reference articles:
❀ Isótopo / Isotopes
❀ Radiactividad / Radioactivity
❀ Ejemplos de Isótopos / Examples of Isotopes
❀ ¿Todos los isótopos de un mismo elemento son radiactivos?
Are all isotopes of the same element radioactive?
❀ Has oído hablar de los isótopos radiactivos
Have you heard of radioactive isotopes?
C R E D I T S (Créditos):
❀ Las imágenes de dominio público fueron reeditadas con las aplicaciones: Paint y PowerPoint, formateadas como archivo PNG
❀ The images (public domain) were re-edited with the applications: Paint and PowerPoint, formatted as PNG file.
❀ Todo este material es producto de una investigación universitaria para la cátedra de Física y Química (L.U.Z.), va dirigido al nivel escolar de primaria y también secundaria, para el agrado y satisfacción de quienes estén solicitando dicha información.
❀All this material is the product of a university research for the Physics and Chemistry (L.U.Z.), it is directed to the primary school level and high school, for the pleasure and satisfaction of those who are requesting this information.

Gracias por compartir este tema Estructura atómica: isótopos y radiactividad
Gracias a usted por tomarse el tiempo y leer mi artículo.
This brings back memories (not necessarily good) of my school days studying Chemistry 🤣😜. !PIZZA
Congratulations @maria1989! You have completed the following achievement on the Hive blockchain and have been rewarded with new badge(s):
Your next target is to reach 1000 replies.
You can view your badges on your board and compare yourself to others in the Ranking
If you no longer want to receive notifications, reply to this comment with the word
STOPCheck out the last post from @hivebuzz:
Support the HiveBuzz project. Vote for our proposal!
I gifted $PIZZA slices here:
@blitzzzz(5/20) tipped @maria1989 (x1)
Please vote for pizza.witness!
Su post ha sido valorado por @ramonycajal
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider delegating to the @stemsocial account (85% of the curation rewards are returned).
You may also include @stemsocial as a beneficiary of the rewards of this post to get a stronger support.
Para darte una opinión fiel y exacta, con la ciencia Física no le entro mucho, la parte química esta bien detallada, me agradó tu explicación de los isótopos y la clasificación en dos tipos (natural y artificial).
Muy bien mi amor! TQM